préparation
Temps de lecture :Le dioxyde de chlore est toujours préparé en solution sur le site d’utilisation par oxydation du chlorite de sodium à l’aide de chlore ou d’acide chlorhydrique (voir dioxyde de chlore).
Dans les deux cas, le pH de mélange des réactifs doit être très acide pour éviter les réactions secondaires qui conduisent rapidement à la formation de l’ion chlorate en milieu neutre.

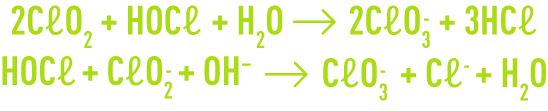
La formation secondaire de chlorate dépend également de la concentration en chlorite du milieu réactionnel ; c’est pourquoi, un autre paramètre déterminant du procédé de production est le rapport des concentrations en chlore et en chlorite.
Le procédé par acidification nécessite 1,25 fois plus de chlorite de sodium et est donc plus coûteux. Le choix entre les deux variantes de production est alors dicté par la possibilité ou non de stockage de chlore. Ces deux procédés nécessitent des préparations et des dispositions spéciales pour en assurer la sécurité (voir dioxyde de chlore).
Outil Marque-page
Cliquez sur l'outil marque-page, puis surlignez le dernier paragraphe lu pour pouvoir poursuivre ultérieurement votre lecture.












