prévention des problématiques liées à la qualité d’eau
Temps de lecture :Stratégie de traitement = mise en oeuvre d'outils. Utiliser les bons outils c'est limiter l'impact environnemental pour une efficacité optimale
En fonction de l’origine de l’eau (eau brute), cours d’eau, lacs, forages, puits, nappes, eau potable (eau de ville) et de l’usage qui sera fait de l’eau sur un site industriel, on sera amené à réaliser un prétraitement pour donner à cette eau brute les qualités nécessaires à son utilisation afin de ne pas gêner le bon fonctionnement des tours de refroidissement. L’eau « adaptée » introduite dans ces tours sera donc dénommée eau d’appoint.
Les prétraitements qui peuvent être appliqués sont :
- dégrillage ;
- coagulation, clarification ;
- chloration, déchloration (charbon actif) ;
- filtration ;
- adoucissement, désalcalinisation, osmose inverse, déminéralisation.
Il existe deux grandes manières de considérer l’eau sur une installation de refroidissement et plus particulièrement les tours aéroréfrigérantes :
- procédé dit d’« équilibre naturel » ou à « pH régulé » : ce procédé consiste à régler pH et TAC de l’eau en circulation, de façon à ce qu’elle soit à l’équilibre calco-carbonique : indice de Ryznar voisin de 6,6. Cela est obtenu par introduction d’acides forts (Acide chlorhydrique, acide sulfurique), et par limitation du taux de concentration. Ce procédé est séduisant par sa simplicité, mais il présente des limites importantes, en particulier :
- la diversité des températures en circuit fait que l’eau ne peut être à l’équilibre en tous points ;
- maintenir un taux de purge important pour limiter la concentration en sels dissous de l’eau en circulation ;
- la perte de CO2 au niveau de la tour déstabilise l’équilibre de l’eau.
- procédé dit à « pH libre » : le pH n’est pas régulé, sa valeur augmentera par rapport à l’eau d’appoint. On laisse l’eau s’équilibrer en fonction des conditions de fonctionnement de l’installation de refroidissement. Cette mise en équilibre induira des phénomènes d’entartrage qui devront être prévenus par des inhibiteurs chimiques.
Dans les sous chapitres qui suivent sont décrits des procédés, des principes actifs qui ont un effet certain qui peut s’avérer insuffisant ou difficile à mettre en œuvre. C’est pourquoi SUEZ, au travers de la gamme aqualead®, propose des solutions de conditionnement reposant sur des formulations.
La mise au point d’une formulation doit prendre en compte :
- l’actif ou les actifs pour l’effet ou les effets que l’on attend ;
- les adjuvants nécessaires pour :
- pour une meilleure solubilisation ;
- une meilleure stabilité au stockage ou dans l’eau à traiter ;
- atteindre plus aisément la cible visée (tensio-actif) ;
- l’éventuelle dangerosité des composants et leurs éventuels impacts sur l'environnement ;
- le coût d’application incluant la mise en œuvre par des équipements simples à élaborer.
la prévention de l’entartrage
La prévention de l’entartrage peut se faire par :
- une modification des caractéristiques des installations de refroidissement: augmentation des vitesses de passage, modification des matériaux, réduction échange thermique, … ;
- une gestion des éléments entartrants : adoucissement total ou partiel, décarbonatation sur résines ou à la chaux, acidification ;
- limitation de la concentration en circuit, ce qui réduit la salinité de l’eau et la concentration en ions intervenants dans les phénomènes d’entartrage.
Cependant, ces mesures préventives sont rarement suffisantes pour prévenir les phénomènes d’entartrage dans les circuits de refroidissement. Le conditionnement est complémentaire et permettra une action complémentaire.
les modes d’inhibition de l’entartrage
Certains produits possèdent des propriétés antitartres car ils agissent en perturbant le phénomène d’entartrage de différentes façons et principalement par :
- séquestration ou complexation : cette réaction est stœchiométrique, les cations divalents (Ca2+, Mg2+, Fe2+, Cu2+…) sont complexés et ne peuvent plus participer à des réactions de précipitation avec certains anions (HCO3-, CO32-, SO42-) ;
- effet de seuil : c’est un effet d’inhibition de la précipitation dès de très faibles concentrations « sous-stœchiométriques » ;
- modification de la cristallisation : ces inhibiteurs modifient la forme des cristaux formés qui sont alors moins adhérents sur les surfaces ;
- dispersion : par cette action les éléments constitutifs du tartre réagissent spécifiquement avec un polymère par voie électrochimique. Ce qui a pour conséquence de les maintenir dispersés et d’éviter leur agglomération et les précipitations.
les principaux inhibiteurs d’entartrage
- les chélatants
Un chélatant agit par complexation ou séquestration.
- les polyphosphates
Les polyphosphates viennent s’absorber sur les germes de cristallisation. Ce sont des modificateurs de cristallisation.
Leur stabilité à la température est relative, lorsque T > 60°C, les molécules s'hydrolysent en orthophosphates, qui n'ont pas le même effet antitartre. Les d'orthophosphates sont facilement métabolisables par les bactéries ce qui peut favoriser des proliférations bactériennes.
- les phosphonates
Les phosphonates agissent par effet de seuil.
Leur stabilité à la température est bonne jusqu’à 180°C.
Les principaux actifs n’ont pas tous la même sensibilité aux biocides oxydants qui peuvent réduire leur efficacité et imposer des surdosages de biocide.
- les polymères
Ce terme regroupe une grande diversité de produits. Leur action est dispersante.
On les distingue en particuliers par leurs poids moléculaires (500 à 20 000) qui influence leur activité : plus le poids moléculaire augmente plus la molécule active est dispersante.
Ces polymères seront plus stables à la température que les phosphonates (> 300°C en général) et présenteront une très bonne résistance au chlore.
les moyens de lutte contre les corrosions
On distingue deux principes pour prévenir la corrosion :
- la protection cathodique ;
- la protection anodique.
Ils permettent de bloquer le processus de corrosion en s’opposant à la migration des ions métalliques vers le milieu environnant.
les inhibiteurs anodiques
les mécanismes et l’application des inhibiteurs anodiques
Les inhibiteurs anodiques sont des composés chimiques qui, par réaction avec les ions métalliques ou avec d’autres ions (ex : Ca2+), sont capables de former un dépôt protecteur sur les surfaces anodiques en s’opposant à la migration des ions métalliques.
Les deux mécanismes possibles sur la surface anodique sont :
- oxydation de la surface du métal pour former un film passivant d’oxydes métalliques;
- blocage de la demi-pile électrochimique par précipitation de sels complexes insolubles (ex : bicarbonate ou phosphate de fer).
Ce mode d’action impose la formation d’un film parfait agissant sur toutes les anodes. En cas de film « imparfait », il y aura une perte de métal qui se concentrera aux anodes restantes, il en résultera une corrosion par piqûres. Il est donc impératif de maintenir une quantité suffisante d’inhibiteur anodique en permanence dans le système de façon à prévenir les piqûres de corrosion. Les inhibiteurs anodiques doivent être utilisés à forte dose (de l'ordre du g/L) souvent réservés aux circuits fermés.
les inhibiteurs anodiques
- les nitrites ;
- les silicates ;
- les molybdates ;
- les orthophosphates ;
- les bicarbonates.
les inhibiteurs cathodiques
les mécanismes et l’application des inhibiteurs cathodiques
La cathode est un point spécifique dans l’installation ce qui n’impose pas de filmer toute la surface de l’installation. Le contrôle des réactions cathodiques est obtenu par formation d’une barrière par précipitation de sels insolubles ce qui permet d’isoler physiquement ces zones de l'eau et de bloquer la réaction cathodique.
Ces inhibiteurs sont plus sûrs que les inhibiteurs anodiques, une corrosion localisée ne se produit pas en cas de sous dosage.
Les dosages à mettre en œuvre sont faibles. Le carbonate de calcium est considéré comme un très bon inhibiteur de corrosion. On forme du carbonate de calcium qui précipite et dépose un film protecteur. Cette réaction est très difficile à contrôler, et dangereuse car le tartre diminue l’échange thermique. C’est pourquoi d'autres inhibiteurs sont utilisés.
les inhibiteurs cathodiques
Leur usage peut être limité de par les limites de concentrations autorisées dans les rejets. Les principaux inhibiteurs cathodiques sont :
- le zinc : très utilisé, peut être associé aux phosphonates, doit être stabilisé pour ne pas précipiter lors de son introduction ;
- les polyphosphates : ils peuvent s'hydrolyser en orthophosphates ;
- les orthophosphates : ils risquent de déposer en quantité trop importante en cas de surdosage ou en présence de THCa élevé ;
- les phosphonates : selon les phosphonates, l’inhibition cathodique est plus ou moins efficace.
les inhibiteurs organiques filmants
L'action de ces composés organiques est liée à la formation d'une fine barrière continue qui isole le métal de l'eau.
Ce type d'inhibiteur présente la particularité d'être efficace en pH acide (jusque 4 ).
- les polyamines grasses : elles sont très peu solubles dans l'eau et se présentent sous forme d'émulsions. Elles peuvent réduire la vitesse de diffusion de l'oxygène ce qui réduit la vitesse de corrosion dans les mêmes proportions ;
- les amines aromatiques : Benzotriazole, Tolyltriazole, Mercaptobenzotriazole : spécifiques pour la protection du cuivre mais aussi des métaux ferreux. Selon les molécules actives il peut y avoir une sensibilité aux biocides oxydants.
la prévention de l’encrassement biologique
les biocides
définition et principes
Les biocides sont les substances actives et les préparations contenant une ou plusieurs substances actives qui sont présentées sous la forme dans laquelle elles sont livrées à l’utilisateur, qui sont destinées à détruire, repousser, ou rendre inoffensifs les organismes nuisibles, à en prévenir l’action ou à les combattre de toute autre manière, par une action chimique ou biologique.
L‘utilisation de biocide n’implique pas de tuer tous les microorganismes présents et/ou visés. Il faut définir l’action recherchée en intégrant l’environnement dans lequel elle devra s’intégrer. La désinfection est une opération au résultat momentané permettant sur les surfaces inertes contaminées d’éliminer ou de tuer les micro-organismes et/ou d’inactiver les virus indésirables, en fonction des objectifs fixés. Le résultat de cette opération est limité aux micro-organismes présents au moment de l’opération.
Avant d’envisager appliquer une formulation biocide il faudra autant que possible dégrader les conditions de croissance.
Sans information, l’injection d’un biocide implique un suivi important ayant pour objet d’apprécier l’effet réellement obtenu et la vitesse de recontamination.
Attention : un biocide ne nettoie pas !
les biocides oxydants
Un biocide oxydant est une formulation qui aura une action oxydante sur d’autres composés chimiques. Ces réactions mettent en œuvre des éléments oxydants tels que le Chlore, le Brome, l’Oxygène. L’action au niveau de la cellule microbienne se traduira par la perturbation ou l’inhibition des métabolismes vitaux.
Les principales caractéristiques des biocides oxydants sont :
- une vitesse d’action élevée 1 à 15 minutes selon la qualité d’eau ;
- une injection continue ;
- un spectre d’action qui concerne toute la matière oxydable, et non pas uniquement les micro-organismes ;
- des doses en fonction du micro-organisme, du temps de contact, de la qualité de l’eau ;
- un pouvoir oxydant qui peut influencer la corrosion ;
- ils peuvent être inactivés.
Du fait de leur réactivité plus ou moins grande, ces formulations peuvent être également utilisées pour d’autres actions tels que déferriser, dégrader ou oxyder des molécules préoccupantes, décolorer…
principe d’utilisation
Le principe d’utilisation consiste à maintenir en permanence le résiduel d’oxydant nécessaire pour obtenir la qualité d’eau voulue du point de vue microbiologique. Leur grande réactivité et la diversité des molécules avec lesquelles une réaction chimique est probable, font qu’il n’est pas possible de connaître quel sera l’ordre des réactions, ni à quel moment l’action biocide se produira parmi l’ensemble des réactions possibles. C’est la raison pour laquelle il faudra déterminer « la demande en oxydant » d’une eau.
les substances les plus souvent utilisées
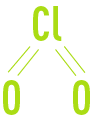
- les précurseurs d’acide hypochloreux : ce sont les formulations, qui en milieu aqueux vont libérer de l’acide hypochloreux : HOCl. Il s’agit du Chlore gazeux (Cl2), de l’extrait de Javel (NaOCl + NaCl), de l’hypochlorite de calcium (CaOCl), des halohydantoïns (BCDMH), des « cyanurates » (ATCC - DCCNa). Les additifs permettant de générer de l’acide hypobromeux sont assimilés à cette famille. Dans l’eau, l’acide hypochloreux sera en équilibre avec l’ion hypochlorite selon la réaction ci-dessous.


La proportion de chaque molécule dépendra de la valeur du pH comme représenté sur la figure 32. Pour des produits bromés le principe est identique mais décalé sur l’échelle de pH comme on peut le constaté sur la figure 33. L’acide hypochloreux et l’acide hypobromeux peuvent aussi intervenir dans des réactions d’addition ou de substitution. Ces réactions représentent une consommation potentielle des actifs.
- molécules actives : seuls l’acide hypochloreux et l’acide hypobromeux ont une activité biocide connue. Plus le pH sera élevé, plus la quantité de précurseurs à mettre en œuvre sera importante.
- Chloramines et Bromamines : Les halogènamines (chloramines et bromamines) aussi appelés « Chlore ou Brome lié ou stabilisé ou encore combiné » en opposition au Chlore ou Brome libre. Ces formulations permettent une meilleure conservation dans le temps. Par contre une fois dans l’eau tout le produit ne libérera pas l’acide hypochloreux en une seule fois. Cette libération selon les formulations et la qualité de l’eau sera plus ou moins rapide. Cela rend la gestion de l’activité du produit plus complexe puisque une augmentation de la dose n’induira pas une augmentation proportionnelle de l’effet.
- intérêts de la Bromation : la dissociation de l’acide hypobromeux dans l’eau en fonction du pH est similaire à celle de l’acide hypochloreux, à la différence que ce phénomène est décalé sur l’échelle de pH, à l’avantage au Brome pour des valeurs croissantes de pH. Le pouvoir oxydant du Brome est proche de celui du Chlore.









- le bioxyde de chlore est très soluble dans l'eau. Sa concentration en solution dépend de la température et de la pression. Il est par ailleurs volatile et peut donc être éliminé facilement par aération. Dans l’eau, le bioxyde de chlore ne réagit pratiquement pas chimiquement avec l'eau. Son activité ne dépendra pas de la valeur du pH. Le bioxyde de chlore un gaz difficilement transportable, il est préparé sur son lieu d'utilisation. La méthode la plus fréquemment utilisée est le mélange proportionné de solutions diluées d’acide chlorhydrique et de chlorite de sodium. Le pouvoir oxydant du bioxyde de chlore est comparable à celui du chlore. Le bioxyde de chlore ne réagira que par oxydo-réduction et aura à ce titre une moindre réactivité à l’égard de la matière organique, comparé à l’extrait de javel. Le bioxyde de chlore ne génère pas de chloramines ni d’autres composés organochlorés constituants des trihalométhanes (THM).

- les précurseurs d’« oxygène » : les formulations sont souvent peu stables au stockage. Elles sont très réactives, mais toutes les voies réactionnelles ne sont pas « à effet biocide », ce qui constitue une perte potentielle au regard de l’effet biocide. Parmi les actifs les plus fréquemment utilisés on trouve :
- le péroxyde d’hydrogène ;
- l’acide péracétique ;
- l’ozone qui nécessite un générateur car ce gaz ne peut être stocké et doit être produit sur site.
les biocides non oxydants dits « biocides de synthèse »
Les biocides de synthèse représentent les formulations qui ne sont pas considérées comme des biocides oxydants.
Ces produits sont généralement utilisés lorsque les conditions ne permettent pas d’utiliser des biocides oxydants.
Les principales caractéristiques des biocides non oxydants sont :
- temps d’action 30 minutes à 24 heures ;
- injection continue ou discontinue ;
- spectre plus ou moins spécifique (algicide, bactéricide, fongicide) ;
- doses en fonction du micro-organisme, du temps de contact, de la qualité de l’eau ;
- peuvent être inactivés.
principes d’utilisation
Les biocides de synthèse peuvent être utilisés en dosage continu ou par « choc ». L’injection d’un choc sur une courte durée d’une dose importante permet d’atteindre ponctuellement sur une courte durée une concentration importante et d’avoir si nécessaire un effet plus intense dans des zones difficilement atteignables comme des biofilms.
La fréquence des chocs est un équilibre entre la dose appliquée, donc l’effet recherché, et la vitesse de recontamination du circuit. Cette dernière sera dépendante des données environnementales qui impliqueront que le circuit est plus ou moins favorable aux développements microbiens.
les substances le plus souvent utilisées
Dans cette famille de produits sont classiquement inclus :
- Organo soufrés (Isothiazoline, thiocarbamate) ;
- Organo-Bromés (BNPD, DBNPA) ;
- Ammonium quaternaires, Aldehydes (Glutaraldéhyde).
Cette liste n’est pas exhaustive et concerne les actifs les plus communément rencontrés dans le domaine du traitement de l’eau.
cas particulier de la génération in-situ
Il est important d’évoquer ce type de technologie qui apporte une réponse à des problématiques liées à la conservation limitée de certains biocides oxydants, ou au stockage de produit dangereux.
génération de bioxyde de chlore
Cette technique est relativement ancienne et maîtrisée. Pour cela il faut utiliser un générateur qui est un appareil sécurisé pour le mélange des deux précurseurs, le plus souvent de l’acide chlorhydrique et du chlorite de sodium, mais ce peut être également de l’acide sulfurique et du chlorite de sodium, ou du chlore gazeux et du chlorite de sodium. Il est recommandé d’utiliser des précurseurs dilués. Les précurseurs ne doivent pas être mis en contact en dehors du générateur, ce qui impose de respecter quelques règles de sécurité.
génération d’acide hypobromeux
Pour produire de l’acide hypobromeux il faut mélanger de l’extrait de Javel et du bromure de sodium. Pour déterminer s’il faut utiliser cette technologie il faut calculer l’intérêt technico-économique, c’est-à-dire rapporter la concentration d’actif pour un pH donné au coût de l’application. Deux cas présentent un intérêt selon la valeur du pH : 100% HOCl ou 100% HOBr. Les autres ratios de mélanges seront moins efficaces pour un même coût ou plus cher pour une même efficacité. Cette technologie présente un intérêt technico-économique lorsque le pH de l’eau à traiter est supérieur à 8,5. Pour des valeurs de pH inférieur l’intérêt est à étudier au cas par cas. En générant 100% d’acide hypobromeux on disposera pour un même pH d’une proportion plus importante d’oxydant libre ACTIF que si l’on utilisait de l’acide hypochloreux (voir figures 32 et 33).
La synthèse du produit doit impérativement se faire sur site et le mélange injecté aussitôt après dans l’eau à traiter, car ce mélange n’est pas stable dans le temps et perdrait en quelques heures toute son efficacité.
génération de monochloramine
Cette technologie permet d’utiliser un précurseur d’aide hypochloreux (HOCl) en cas de très forte demande en oxydant d’une eau à traiter. Ainsi l’activité du produit est plus centrée sur l’action biocide et les pertes d’actif dues à la grande réactivité de l’HOCl sont limitées. Cette technologie pourra être envisagée pour des applications en sidérurgie, ou pour des eaux très contaminées par de la matière organique.
La synthèse du produit doit impérativement se faire sur site et le mélange injecté aussitôt après dans l’eau à traiter, car ce mélange n’est pas stable dans le temps et perdrait rapidement toute son efficacité. Les conditions de mélange : les précurseurs à utiliser doivent être connus et maîtriser pour éviter tout risque de dégazages ou des réactions exothermiques.
génération de chlore par électrolyse
Cette technologie met en œuvre un précurseur non dangereux (chlorure de sodium) et très stable dans le temps. Cela réduit considérablement les risques liés à l’usage des produits chimiques si l’on compare aux biocides en général ou à l’extrait de Javel ou le chlore gazeux. Cette stabilité et sécurisation induit des réductions de coût significative. Le chlore produit passe sous forme d’acide hypochloreux dans l’eau. Comparé à l’extrait de Javel il n’y a pas de sous-produits associés tels que sels, chlorates etc...






les techniques physiques
les Ultra-Violets
Les U.V. sont des rayonnements spécifiques produits par des lampes qui nécessitent d’être dimensionnée en terme de puissance et donc d’effet recherché au regard de la qualité d’eau. Les paramètres à considérer sont les MES , la transmittance, la contamination microbienne, la concentration en matière oxydable. Un entretien (nettoyage et changement des lampes) est à prévoir. Il existe plusieurs types d’UV, seuls les UVc ont un pouvoir biocide. Ils présentent une sensibilité à la température de l’eau : optimum 20°C. L’action des UV se situe au niveau de l’ADN des micro-organismes. L’automatisation et l’adaptation à l’évolution de la qualité de l’eau très difficile et complexe. Les UV n’induisent pas ou très peu de modification de la qualité de l’eau.
Si les ultra-violets peuvent rationaliser l’usage des biocides, ils ne peuvent pas pour autant s’y substituer.
Bien que l’efficacité des UV ne soit plus à démontrer, leur action reste localisée à l’emplacement de la lampe sur un circuit, et l’activité biocide ne peut être « exportée », transporter vers des zones contaminées distantes.
les ultrasons
Les ultra-sons sont une vibration physique produite par un courant électrique dans une chambre. Cette vibration sera caractérisée par son amplitude et sa fréquence. Selon ces caractéristiques on produira des bulles d’air ou bien vides qui seront déstructurantes. Ce sont les bulles de vide qui seront plus efficaces et permettront d’avoir un effet biocide plus important. L’action consiste à déstructurer et désorganiser la cohésion cellulaire des bactéries. Comme pour les UV, l’installation (chambre de réaction) devra être dimensionnée en fonction de la qualité d’eau. Les paramètres à considérer sont les MES , la transmittance, la contamination microbienne, la concentration en matière oxydable et en matière organique.
Si les ultrasons peuvent rationaliser l’usage des biocides, ils ne peuvent pas pour autant s’y substituer.
Bien que l’efficacité des ultrasons ne soit plus à démontrer, leur action reste localisée à l’emplacement de la chambre sur un circuit, et l’activité biocide ne peut être « exportée », transporter vers des zones contaminées distantes.
L’utilisation des ultrasons peut induire un réchauffement de l’eau traitée de 1°C environ.
les techniques connexes : les produits tensio-actifs
Les termes couramment utilisés pour ces formulations sont biodispersants et biodétergents. Il s'agit d'une famille de produits qui ont diverses propriétés. Les biodispersants ou biodétergents n'ont généralement pas de pouvoir biocide. Les formulations sont tensio-actives et modifient les caractéristiques physiques de l'eau traitée en changeant la tension superficielle exercée sur les surfaces.
Une molécule tensio-active comporte deux parties:
- un groupe polaire qui possède une affinité pour l'eau (hydrophile) ;
- un groupe apolaire (hydrophobe) ou peu polaire, qui possède une affinité pour les corps gras.
Les actifs sont classés en fonction de la nature de la partie polaire:
- anionique ;
- non ionique ;
- cationique ;
- amphotère.
La structure des tensio-actifs leur confère des propriétés :
- électrochimique : molécules anioniques ou cationiques réagissant avec des sites de charge opposée. Cette propriété contribue à augmenter la mouillabilité des dépôts et à les fragiliser mécaniquement;
- de solubilisation ou hydrotrope : action visant à rendre soluble un élément souillant ou une partie de cet élément. Les biofilms peuvent contenir des éléments peu ou pas solubles tels que lipides, protéines... Les actifs utilisés auront un pôle hydrophile et un pôle hydrophobe;
- mouillant : contribue à accroître la pénétrabilité de l'eau au sein d'une structure organique complexe. L'action se concrétise par une modification de la tension superficielle (on augmente la surface d'étalement d'une goutte d'eau).
- dispersant : pour éviter l'agglomération et maintenir en suspension;
- détergent : processus de « désolidarisation » d'un élément de son support.
Ces propriétés sont exploitées pour éliminer le biofilm ou ralentir sa formation dans les installations de refroidissement. Elles peuvent être complémentaires de l’action biocide et permettre aux biocides d’avoir un effet en des zones difficile d’accès.
Pour être pleinement efficace, un traitement tensioactif doit être associé à un effet mécanique généralement produit par le flux d'eau. Le démarrage d'un traitement tensioactif peut contribuer à fragiliser des structures biofilm et ainsi remettre en circulation une flore plus ou moins importante et jusque-là fixée. Ces périodes doivent faire l'objet d'une surveillance accrue et d'un renforcement du traitement biocide associé.
Quand un effet tensio-actif est revendiqué au travers de l'utilisation d'un biodispersant ou d'un biodétergent, le produit devra satisfaire aux exigences du règlement n° 648-2004, modifié par le règlement UE 907-2006, relatif aux détergents.
Le choix de la stratégie de traitement intègre les contraintes réglementaires, en particulier les textes relatifs à l'environnement, à l'eau, aux rejets et aux biocides.
Outil Marque-page
Cliquez sur l'outil marque-page, puis surlignez le dernier paragraphe lu pour pouvoir poursuivre ultérieurement votre lecture.












