pollution induite par les traitements
Temps de lecture :L’introduction d’un réactif dans l’eau peut conduire à deux formes de pollution : les impuretés du réactif lui-même et les produits de réaction du réactif avec les matières organiques de l’eau.
impuretés dues au réactif
Dans de nombreux pays, l’utilisation d’un réactif est soumise à l’agrément des autorités sanitaires. La législation peut prévoir, pour chaque réactif, une concentration maximale d’impuretés à respecter par le producteur. Une analyse précise des produits doit être effectuée. Au cas où l’on constate la présence d’impuretés, il importe de vérifier que la chaîne de traitement prévue en permet l’élimination.
coagulant
Certains coagulants sont préparés à partir de minerais ou métaux pouvant contenir des impuretés en quantité non négligeable : attaque acide de bauxite pour préparer le sulfate d’aluminium, attaque de ferrailles pour préparer le chlorure ferrique. Cette attaque dissout également des impuretés (tungstène, manganèse, arsenic).
D’autres coagulants sont préparés à partir de sous-produits d’une autre industrie. Le chlorosulfate ferrique, préparé à partir de sulfate ferreux provenant de l’industrie du titane, peut contenir une quantité relativement importante de manganèse.
polyélectrolytes, adjuvants
Les polyélectrolytes de synthèse sont préparés par polymérisation de monomères (ex. : acrylamides, amines…).
En traitement d’ EP, la législation de chaque pays peut fixer le type de monomère utilisable, la teneur maximale en monomère résiduel tolérable dans le polymère et/ou le taux de traitement maximal qu’il est possible de mettre en œuvre (en France dans le cas des polyacrylamides : 0,025 % de monomère acrylamide et 0,4 mg·L–1 comme dose maximale utilisable afin de respecter la valeur paramétrique européenne de 0,1 µg·L–1 dans l’eau distribuée).
chlore et dérivés
Suivant son origine, le chlore liquide, en particulier, contient parfois diverses impuretés telles que : Br2, CCℓ4, CHCℓ3, HCℓ et hexachloroéthane, hexachlorobenzène, sels de fer.
De même le CℓO2, suivant sa méthode de préparation, contient plus ou moins de chlorite et chlorate, et lors de sa réaction avec les MO de l’eau il « rétrograde » à l’état de chlorite. L’hypochlorite de sodium (eau de javel) contient aussi des chlorates.
chaux – correction de pH
La chaux vive ou éteinte a rarement une pureté supérieure à 93 % et ses impuretés (essentiellement insolubles : CaCO3, SiO2…) peuvent contribuer de manière importante à la turbidité de l’eau potable si de l’eau de chaux clarifiée dans un saturateur n’est pas employée.
sous-produits d’oxydation
Au chap. Oxydation et réduction, les mécanismes réactionnels entre les divers oxydants-désinfectants utilisés et les différents polluants des eaux sont décrits.
Comme souligné au impuretés organiques, l’introduction d’oxydant (Cℓ2, H2O2, O3) comme agent désinfectant, en réagissant principalement sur les matières organiques des eaux, peut créer des sous-produits d’oxydation (ex. : THM, HAA, HAN…) dont certains sont dangereux pour la santé humaine (effets cancérigène et/ou mutagène), d’autres sont sources de désagrément (goût…). C’est principalement le cas du chlore et de l’hypochlorite, mais il n’existe aucun oxydant sans sous-produit d’oxydation ; par exemple l’ozone dans certains domaines de pH, température (voir oxydation et désinfection par l'ozone), peut oxyder Br– en bromate (VP = 10 µg·L–1).
La réaction de formation des THM peut se faire soit directement par l’action du chlore présent dans l’eau sous forme CℓO–, soit par un autre halogène (brome ou iode), qui peut avoir été déplacé par le chlore sous forme XO–, selon la réaction de base :


Les matières organiques carbonées qui donnent lieu à cette réaction sont principalement les méthylcétones, ou, d’une manière plus générale, tous les produits organiques qui, par oxydation, peuvent être oxydés en méthylcétones. Ces précurseurs de THM se rencontrent principalement dans les substances humiques et dans les MO d’origine algale.
La chloration des matières organiques conduit également à la formation d’autres composés qui n’ont pas été encore, à ce jour, tous identifiés (figure 10). Ces sous-produits d’oxydation sont maintenant systématiquement recherchés, et leur teneur encadrée par des normes évolutives et variables suivant les pays.

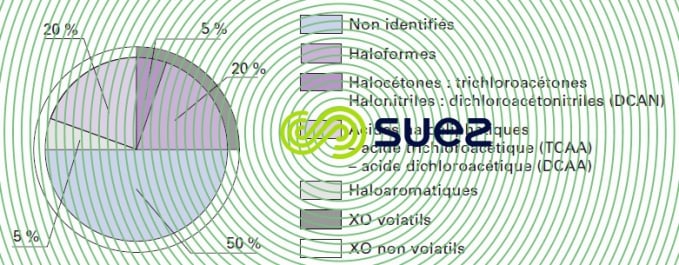

Les filières de traitement modernes (voir Traitement des eaux potables) sont conçues pour limiter au maximum ces sous-produits. Toutefois, comme le souligne l’OMS, cette recherche ne doit pas être faite au détriment d’une bonne désinfection (ex. : choléra au Pérou en 1991).
Outil Marque-page
Cliquez sur l'outil marque-page, puis surlignez le dernier paragraphe lu pour pouvoir poursuivre ultérieurement votre lecture.












